Submukosale svulster (SMT) i mage-tarmkanalen er forhøyede lesjoner som stammer fra muscularis mucosa, submucosa eller muscularis propria, og kan også være ekstraluminale lesjoner. Med utviklingen av medisinsk teknologi har tradisjonelle kirurgiske behandlingsalternativer gradvis gått inn i en æra med minimalt invasiv behandling, som for eksempel laparoskopisk kirurgi og robotkirurgi. I klinisk praksis kan man imidlertid se at «kirurgi» ikke er egnet for alle pasienter. I de senere årene har verdien av endoskopisk behandling gradvis fått oppmerksomhet. Den nyeste versjonen av den kinesiske ekspertkonsensusen om endoskopisk diagnose og behandling av SMT er utgitt. Denne artikkelen vil kort beskrive relevant kunnskap.
1. SMT-epidemisk karakterristiske
(1) Forekomsten av SMT er ujevn i ulike deler av fordøyelseskanalen, og magen er det vanligste stedet for SMT.
Forekomsten av diverseDeler av fordøyelseskanalen er ujevnt fordelt, med den øvre delen av fordøyelseskanalen som den vanligste. Av disse forekommer 2/3 i magesekken, etterfulgt av spiserøret, tolvfingertarmen og tykktarmen.
(2) Det histopatologiskel typer SMT er komplekse, men de fleste SMT er godartede lesjoner, og bare få er ondartede.
A.SMT inkluderer ingenn-neoplastiske lesjoner som ektopisk bukspyttkjertelvev og neoplastiske lesjoner.
B. Blant de neoplastiske lesjonenes, gastrointestinale leiomyomer, lipomer, Brucella-adenomer, granulosacelletumorer, schwannomer og glomustumorer er for det meste godartede, og mindre enn 15 % kan fremstå som vev Lær ondt.
C. Gastrointestinal stromal-svulster (GIST) og nevroendokrine svulster (NET) ved SMT er svulster med et visst malignt potensial, men dette avhenger av størrelse, plassering og type.
D. Plasseringen av SMT er relaterttil den patologiske klassifiseringen: a. Leiomyomer er en vanlig patologisk type SMT i spiserøret, og står for 60 % til 80 % av øsofageale SMT-er, og forekommer oftere i midtre og nedre segmenter av spiserøret; b. De patologiske typene av gastrisk SMT er relativt komplekse, med GIST, leiomyoc. ma og ektopisk bukspyttkjertel er de vanligste. Blant gastrisk SMT finnes GIST oftest i fundus og magesekken, leiomyom er vanligvis lokalisert i cardia og øvre del av kroppen, og ektopisk bukspyttkjertel og ektopisk bukspyttkjertel er vanligst. Lipomer er vanligere i magesekkens antrum; c. Lipomer og cyster er vanligere i de nedadgående og bulbøse delene av tolvfingertarmen; d. Ved SMT i den nedre mage-tarmkanalen er lipomer dominerende i tykktarmen, mens NET-er er dominerende i endetarmen.
(3) Bruk CT og MR til å gradere, behandle og evaluere svulster. For SMT-er som mistenkes for å være potensielt ondartede eller har store svulster (langediameter > 2 cm), anbefales CT og MR.
Andre bildediagnostiske metoder, inkludert CT og MR, er også av stor betydning for diagnostisering av SMT. De kan direkte vise plasseringen av svulstens forekomst, vekstmønster, lesjonsstørrelse, form, tilstedeværelse eller fravær av lobulasjon, tetthet, homogenitet, grad av forsterkning og grensekontur, osv., og kan finne om og graden av tykkhet.åpning av mage-tarmveggen. Enda viktigere er det at disse bildediagnostiske undersøkelsene kan oppdage om det er invasjon av tilstøtende strukturer i lesjonen og om det er metastase i omkringliggende bukhinne, lymfeknuter og andre organer. De er den viktigste metoden for klinisk gradering, behandling og prognostisk vurdering av svulster.
(4) Vevsprøvetaking anbefales ikkeAnbefales for godartede SMT-er som kan diagnostiseres ved konvensjonell endoskopi kombinert med EUS, som lipomer, cyster og ektopisk bukspyttkjertel.
For lesjoner som mistenkes å være ondartede, eller når konvensjonell endoskopi kombinert med EUS ikke kan vurdere de godartede eller ondartede lesjonene, kan EUS-veiledet finnålsaspirasjon/biopsi brukes (endoskopisk ultralydveiledet finnålsaspirasjon).Nåleaspirasjon/biopsi, EUS-FNA/FNB), slimhinnesnittbiopsi (mukosal insisjonsassistert biopsi, MIAB), osv. utfører biopsiprøvetaking for preoperativ patologisk evaluering. I lys av begrensningene ved EUS-FNA og den påfølgende effekten på endoskopisk reseksjon, kan enheter med moden endoskopisk behandlingsteknologi behandles av erfarne pasienter som er kvalifisert for endoskopisk kirurgi, forutsatt at svulsten kan resekteres fullstendig. Endoskopisten utfører endoskopisk reseksjon direkte uten å innhente en preoperativ patologisk diagnose.
Enhver metode for å innhente patologiske prøver før kirurgi er invasiv og vil skade slimhinnen eller forårsake adhesjon til submukosalt vev, og dermed øke vanskelighetsgraden ved kirurgi og muligens øke risikoen for blødning, perforasjon.rasjon og tumorspredning. Derfor er preoperativ biopsi ikke nødvendigvis nødvendig. Det er nødvendig med vevsprøvetaking, spesielt for SMT-er som kan diagnostiseres ved konvensjonell endoskopi kombinert med EUS, som lipomer, cyster og ektopisk bukspyttkjertel.
2. SMT endoskopisk behandlingnt
(1) Behandlingsprinsipper
Lesjoner som ikke har lymfeknutemetastase eller svært lav risiko for lymfeknutemetastase, kan fjernes fullstendig ved hjelp av endoskopiske teknikker, og har lav risiko for gjenværende tumor og tilbakefall, og er egnet for endoskopisk reseksjon hvis behandling er nødvendig. Fullstendig fjerning av svulsten minimerer gjenværende tumor og risikoen for tilbakefall.Prinsippet om tumorfri behandling bør følges under endoskopisk reseksjon, og tumorkapselens integritet bør sikres under reseksjonen.
(2) Indikasjoner
i. Svulster med ondartet potensial mistenkt ved preoperativ undersøkelse eller bekreftet ved biopsipatologi, spesielt de som mistenkes for gastrointestinal sykdomST med en preoperativ vurdering av en tumorlengde på ≤2 cm og lav risiko for tilbakefall og metastase, og med mulighet for fullstendig reseksjon, kan endoskopisk resekteres; for svulster med lang diameter. Ved mistenkt lavrisiko-GIST >2 cm, hvis lymfeknute- eller fjernmetastase er ekskludert fra preoperativ evaluering, under forutsetning av å sikre at svulsten kan resekteres fullstendig, kan endoskopisk kirurgi utføres av erfarne endoskopister i en enhet med moden endoskopisk behandlingsteknologi.
ii. Symptomatisk (f.eks. blødning, obstruksjon) SMT.
iii. Pasienter hvis svulster mistenkes å være godartede ved preoperativ undersøkelse eller bekreftes av patologi, men som ikke kan følges opp regelmessig, eller hvis svulster forstørres i løpet av kort tid i oppfølgingsperioden og som har et sterkt ønske ome for endoskopisk behandling.
(3) Kontraindikasjoner
i. Identifiser lesjonene som har megsmaksifisert til lymfeknuter eller fjerne steder.
ii. For noen SMT med klar lymfenodeeller fjernmetastase, er bulkbiopsi nødvendig for å fastslå patologi, noe som kan betraktes som en relativ kontraindikasjon.
iii. Etter detaljert preoperativ behandlingevaluering fastslår det at allmenntilstanden er dårlig, og endoskopisk kirurgi er ikke mulig.
Godartede lesjoner som lipom og ektopisk bukspyttkjertel forårsaker vanligvis ikke symptomer som smerte, blødning og obstruksjon. Når SMT manifesterer seg som erosjon, sår eller øker raskt i løpet av kort tid, muligheten for at det er en ondartet lesjon øker.
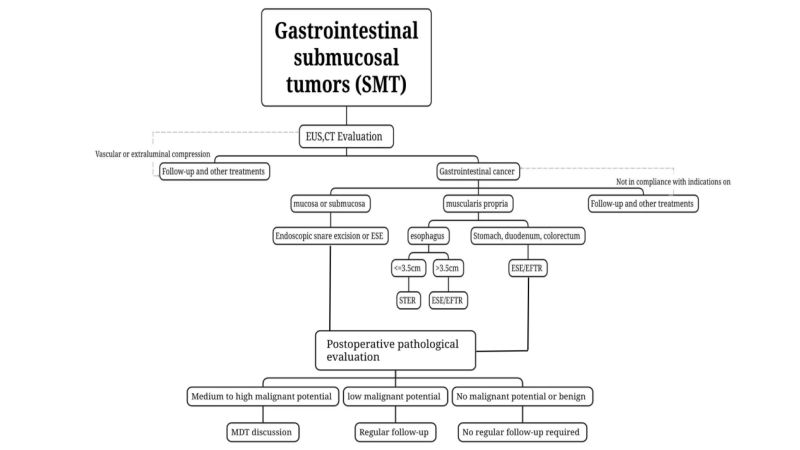
(4) Valg av reseksjonsmetoded
Endoskopisk snare-reseksjon: ForSMT som er relativt overfladisk, stikker ut i hulrommet som bestemt av preoperative EUS- og CT-undersøkelser, og kan resekteres fullstendig på én gang med en snare, kan endoskopisk snarereseksjon brukes.
Innenlandske og utenlandske studier har bekreftet at det er trygt og effektivt ved overfladisk SMT <2 cm, med en blødningsrisiko på 4 % til 13 % og perforasjon.risiko på 2 % til 70 %.
Endoskopisk submukosal ekskavning, ESE: For SMT-er med lang diameter ≥2 cm eller hvis preoperative bildediagnostiske undersøkelser som EUS og CT bekrefterNår svulsten stikker ut i hulrommet, er ESE mulig for endoskopisk ermetreseksjon av kritiske SMT-er.
ESE følger de tekniske vanene tilendoskopisk submukosal disseksjon (ESD) og endoskopisk slimhinnereseksjon, og bruker rutinemessig et sirkulært «flip-top»-snitt rundt svulsten for å fjerne slimhinnen som dekker SMT-en og eksponere svulsten fullstendig. , for å oppnå formålet med å bevare svulstens integritet, forbedre radikaliteten til kirurgi og redusere intraoperative komplikasjoner. For svulster ≤1,5 cm kan en fullstendig reseksjonsrate på 100 % oppnås.
Submukosal tunnelering endoskopisk resektion, STER: For SMT som stammer fra muscularis propria i spiserøret, hilum, den mindre krumningen av magesekken, gastrisk antrum og endetarm, som er lette å etablere tunneler i, og den tverrgående diameteren er ≤ 3,5 cm, kan STER være den foretrukne behandlingsmetoden.
STER er en ny teknologi utviklet basert på peroral endoskopisk øsofageal sfinkterotomi (POEM) og er en utvidelse av ESD-teknologi.En bloc-reseksjonsraten for STER for SMT-behandling når 84,9 % til 97,59 %.
Endoskopisk fulltykkelsesresektion,EFTR: Den kan brukes til SMT der det er vanskelig å etablere en tunnel eller der den maksimale tverrgående diameteren til svulsten er ≥3,5 cm og ikke er egnet for STER. Hvis svulsten stikker ut under den lilla membranen eller vokser utenfor en del av hulrommet, og svulsten finner seg å være tett festet til serosalaget under operasjonen og ikke kan separeres, kan den brukes. EFTR utfører endoskopisk behandling.
Riktig suturering av perforasjonenStedet etter EFTR er nøkkelen til suksess med EFTR. For å kunne vurdere risikoen for tilbakefall av tumor nøyaktig og redusere risikoen for spredning av tumor, anbefales det ikke å kutte og fjerne den resekterte tumorprøven under EFTR. Hvis det er nødvendig å fjerne tumoren i biter, må perforasjonen repareres først for å redusere risikoen for tumorsåing og -spredning. Noen sutureringsmetoder inkluderer: metallklipssutur, sugeklipssutur, omental patch-suturteknikk, "purse bag sutur"-metoden med nylontau kombinert med metallklips, rake metal clip closure system (over the scope clip, OTSC), OverStitch-sutur og andre nye teknologier for å reparere gastrointestinale skader og håndtere blødninger, etc.
(5) Postoperative komplikasjoner
Intraoperativ blødning: Blødning som fører til at pasientens hemoglobinnivå faller med mer enn 20 g/L.
For å forhindre massiv intraoperativ blødning,Tilstrekkelig submukosal injeksjon bør utføres under operasjonen for å eksponere større blodårer og legge til rette for elektrokoagulasjon for å stoppe blødning. Intraoperativ blødning kan behandles med forskjellige snittkniver, hemostatiske tang eller metallklips, og forebyggende hemostase av eksponerte blodårer som finnes under disseksjonsprosessen.
Postoperativ blødning: Postoperativ blødning manifesterer seg som oppkast av blod, melena eller blod i avføringen. I alvorlige tilfeller kan hemoragisk sjokk forekomme. Det forekommer vanligvis innen 1 uke etter operasjonen, men kan også forekomme 2 til 4 uker etter operasjonen.
Postoperativ blødning er ofte relatert tilfaktorer som dårlig postoperativ blodtrykkskontroll og korrosjon av gjenværende blodkar forårsaket av magesyre. I tillegg er postoperativ blødning også relatert til sykdommens plassering, og er vanligere i magesårene og nedre endetarm.
Forsinket perforasjon: Manifesterer seg vanligvis som oppblåst mage, forverrede magesmerter, tegn på peritonitt, feber, og bildediagnostikk viser gassansamling eller økt gassansamling sammenlignet med tidligere.
Det er hovedsakelig relatert til faktorer som dårlig suturering av sår, overdreven elektrokoagulasjon, å stå opp for tidlig for å bevege seg, å spise for tidlig, dårlig blodsukkerkontroll og erosjon av sår forårsaket av magesyre. a. Hvis såret er stort eller dypt, eller såret har fissikker-lignende forandringer, bør sengetid og fastetid forlenges passende, og gastrointestinal dekompresjon bør utføres etter operasjonen (pasienter etter kirurgi i nedre mage-tarmkanal bør ha analkanaldrenasje); b. Diabetespasienter bør kontrollere blodsukkeret strengt; de med små perforasjoner og milde thorax- og abdominale infeksjoner bør gis behandlinger som faste, antiinfeksjonsmiddel og syresuppresjon; c. For de med effusjon kan lukket thoraxdrenasje og abdominalpunksjon utføres. Slanger bør plasseres for å opprettholde jevn drenasje; d. Hvis infeksjonen ikke kan lokaliseres etter konservativ behandling eller kombineres med alvorlig thorax-abdominal infeksjon, bør kirurgisk laparoskopi utføres så snart som mulig, og perforasjonsreparasjon og abdominal drenasje bør utføres.
Gassrelaterte komplikasjoner: Inkludert subkutanneoøst emfysem, pneumomediastinum, pneumothorax og pneumoperitoneum.
Intraoperativt subkutant emfysem (vist som emfysem i ansikt, hals, brystvegg og pung) og mediastinalt pneumofysem (shevelse i epiglottis kan oppdages under gastroskopi) krever vanligvis ikke spesiell behandling, og emfysemet vil vanligvis gå over av seg selv.
Alvorlig pneumothorax oppstår dunder operasjonen [luftveistrykket overstiger 20 mmHg under operasjonen]
(1 mmHg = 0,133 kPa), SpO2 < 90 %, bekreftet med akutt røntgen av brystkassen ved sengen], kan kirurgi ofte fortsette etter lukket thoraxdrainagealder.
For pasienter med tydelig pneumoperitoneum under operasjonen, bruk en pneumoperitoneumnål for å punktere McFarland-punktet.i høyre nedre del av magen for å tømme luften, og la stikknålen være på plass til operasjonen er avsluttet, og fjern den deretter etter å ha bekreftet at ingen åpenbar gass slippes ut.
Gastrointestinal fistel: Fordøyelsesvæske forårsaket av endoskopisk kirurgi strømmer inn i brystet eller bukhulen gjennom en lekkasje.
Esophageale mediastinale fistler og øsofagothorakale fistler er vanlige. Når en fistel oppstår, utfør lukket thoraxdrenasje for å opprettholdei jevn drenering og gi tilstrekkelig ernæringsstøtte. Om nødvendig kan metallklips og forskjellige lukkeanordninger brukes, eller hele dekselet kan resirkuleres. Stenter og andre metoder brukes til å blokkerefistel. Alvorlige tilfeller krever rask kirurgisk inngrep.
3. Postoperativ behandling (foppfølging)
(1) Godartede lesjoner:Patologiantyder at godartede lesjoner som lipom og leiomyom ikke krever obligatorisk regelmessig oppfølging.
(2) SMT uten ondsinnetmaurpotensial:For eksempel, rektale NET-er på 2 cm og GIST med middels og høy risiko, bør fullstendig stadieinndeling utføres og tilleggsbehandlinger (kirurgi, kjemoradioterapi, målrettet terapi) bør vurderes sterkt. Utformingen av planen bør være basert på tverrfaglig konsultasjon og på individuell basis.
(3) Lavt malignt potensial SMT:For eksempel må lavrisiko-GIST evalueres med EUS eller bildediagnostikk hver 6. til 12. måned etter behandling, og deretter behandles i henhold til kliniske instruksjoner.
(4) SMT med middels og høyt malignt potensial:Hvis postoperativ patologi bekrefter type 3 gastrisk NET, kolorektal NET med en lengde >2 cm og GIST med middels og høy risiko, bør fullstendig stadieinndeling utføres og tilleggsbehandlinger (kirurgi, kjemoradioterapi, målrettet terapi) bør vurderes sterkt. Utformingen av planen bør være basert på[om oss 0118.docx] tverrfaglig konsultasjon og på individuell basis.
Vi, Jiangxi Zhuoruihua Medical Instrument Co., Ltd., er en produsent i Kina som spesialiserer seg på endoskopiske forbruksvarer, som for eksempelbiopsi-tang, hemoklips, polypp snare, skleroterapinål, spraykateter, cytologibørster, styretråd, kurv for steinutvinning, nasal galledrenasjekateterosv. som er mye brukt iEMR, ESD,ERCPProduktene våre er CE-sertifiserte, og fabrikkene våre er ISO-sertifiserte. Varene våre har blitt eksportert til Europa, Nord-Amerika, Midtøsten og deler av Asia, og har oppnådd bred anerkjennelse og ros fra kunder!
Publisert: 18. januar 2024


